廣東工藝特異型宿主細胞蛋白(HCP)殘留檢測抗體覆蓋率驗證
來源:
發(fā)布時間:2025-08-25
大腸埃希氏菌(Escherichia coli,E. coli )又稱大腸桿菌,其作為模式微生物被廣泛應用于生命科學研究中。大腸桿菌是表達藥用異源蛋白的常用微生物,在被批準的藥用蛋白中,大約30%的產(chǎn)品以大腸桿菌作為表達宿主菌。與其他表達平臺一樣,盡管下游復雜的純化步驟已經(jīng)去除了大量的雜質(zhì),但終產(chǎn)品中仍會存在HCP殘留風險,必須對其進行質(zhì)量控制,使其符合放行標準。湖州申科生物E.coli表達菌HCP殘留檢測試劑盒用于大腸桿菌表達菌株BL21來源的宿主細胞蛋白定量檢測,適用于重組蛋白類產(chǎn)品的工藝中間品和原液類樣品,如白細胞介素(IL)、干擾素(rhIFN)、粒細胞-巨噬細胞集落刺激因子(rhGM-CSF)、腫瘤壞死因子(rhTNF)、促生長因子(EGF/FGF/PDGF)等。試劑盒檢測步驟少,快速,專一性強,性能穩(wěn)定可靠。
湖州申科系列HCP檢測產(chǎn)品均進行了校準品的表征分析,抗體覆蓋率分析。廣東工藝特異型宿主細胞蛋白(HCP)殘留檢測抗體覆蓋率驗證
湖州申科在宿主細胞蛋白(HCP)ELISA檢測技術(shù)領(lǐng)域擁有深厚的積累,已成功構(gòu)建高質(zhì)量、全流程的自有開發(fā)平臺,覆蓋HCP檢測試劑盒研發(fā)的關(guān)鍵環(huán)節(jié):①抗原表征與制備:基于合規(guī)平臺的HCP Reference/Antigen制備能力,采用2D凝膠電泳等先進技術(shù)確保抗原庫的代表性。②動物免疫與抗體制備:依托自有免疫動物平臺,控制免疫原設(shè)計與動物免疫過程,產(chǎn)出高特異性、廣覆蓋度的抗體。③體系開發(fā)與驗證:憑借成熟的技術(shù)經(jīng)驗開發(fā)高靈敏度、高穩(wěn)定性的檢測體系,并嚴格遵循GMP標準完成方法學驗證。該平臺通過全流程自主可控的技術(shù)整合,從源頭保證試劑盒性能的一致性與可靠性,明顯降低不同批次試劑盒的檢測變異性。其研發(fā)的HCP ELISA試劑盒已成功服務(wù)于國內(nèi)外200余家生物醫(yī)藥企業(yè),為生物制品(如單抗、疫苗)的工藝開發(fā)、質(zhì)量控制及法規(guī)申報(如IND/BLA)提供符合監(jiān)管要求的定制化檢測解決方案。
畢赤酵母宿主細胞蛋白(HCP)殘留檢測免疫策略定制化宿主細胞蛋白殘留檢測試劑盒產(chǎn)生的HCP抗體特異性更好,能檢出高風險HCP。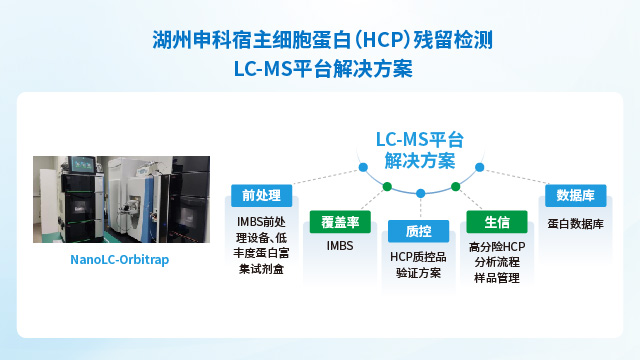
湖州申科生物CHO-K1 HCP 殘留檢測試劑盒(一步酶聯(lián)免疫吸附法)基于固相酶聯(lián)免疫吸附分析法,適用于基于CHO-K1細胞生產(chǎn)的生物制品中宿主殘留蛋白的定量檢測。該分析方法通過在預包被抗CHO-K1HCPs綿羊多抗的酶標板中加入校準品或待測樣品、HRP標記的抗CHO-K1HCPs綿羊多抗進行共孵育。洗滌后,加入TMB底物進行顯色反應,再使用終止液終止酶催化反應。利用酶標儀在450nm波長下測讀吸光度,其吸光度與校準品或待測樣品中的HCPs濃度成正相關(guān),通過校準品擬合的劑量-反應曲線即可計算得出待測樣品中HCPs的濃度。本試劑盒對待測樣品無需進行特殊處理,只需通過合適的稀釋比例進行適用性驗證即可直接使用。本試劑盒操作步驟少,快速,檢測專一性強,性能穩(wěn)定可靠。
影響宿主細胞蛋白(HCP)殘留檢測結(jié)果的因素之一是方法選擇。酶聯(lián)免疫吸附法(ELISA法)和液相色譜-質(zhì)譜聯(lián)用方法(LC-MS法)是目前HCP檢測的兩大常用方法。文獻統(tǒng)計顯示,目前對于總HCP定量,ELISA仍是主流方法;MS法作為對特定蛋白(例如,高風險蛋白)的鑒定和定量,已成為重要的互補手段。此外檢測過程中使用的試劑和耗材的質(zhì)量直接影響檢測結(jié)果的準確性。低質(zhì)量的試劑可能導致假陽性或假陰性結(jié)果。例如,抗體的特異性和親和力不足,可能導致ELISA檢測中的交叉反應;抗原代表性不強或是抗體覆蓋率低,可能會導致漏檢;稀釋液抗干擾能力弱,可能影響檢測準確性。案例研究表明,采用定制化方法替代原有商業(yè)化試劑盒后,抗原代表性和抗體覆蓋率明顯提高,HCP檢測值整體升高。
湖州申科可根據(jù)客戶要求,快速定制符合用戶生產(chǎn)工藝的HCP商業(yè)化檢測試劑盒,滿足用戶快速替換的檢測需求。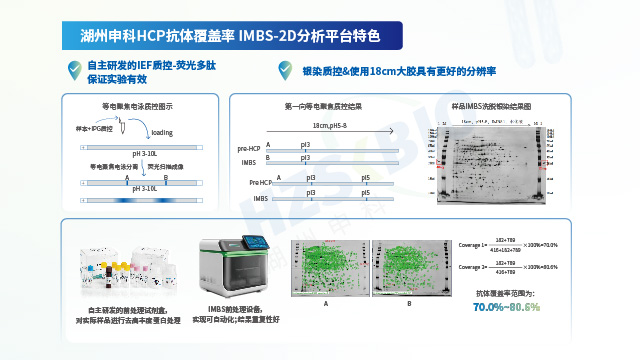
LC-MS技術(shù)作為生物制品宿主細胞蛋白殘留檢測新趨勢,需考慮以下幾點:①穩(wěn)定性:需要HCPs LC-MS檢測流程進行驗證,全流程都需要有嚴格的QC控制,確保檢測結(jié)果的一致性和穩(wěn)定性。②可重復性:不同類型生物制品中HCPs提取效率不同,不同人員操作存在差異,需要在上機前通過不同方法評估HCPs的提取效率,避免人為因素造成結(jié)果重復性差。③準確度:方法開發(fā)與驗證階段,通過設(shè)立內(nèi)標與定量算法,根據(jù)內(nèi)標響應回算得到HCPs的含量,確保定量結(jié)果的準確性。④抗干擾能力:高豐度蛋白和特殊基質(zhì)會對質(zhì)譜檢測產(chǎn)生影響,需要通過前處理手段對高豐度蛋白或特殊的基質(zhì)進行去除,以減少其對HCPs肽段在質(zhì)譜檢測時的影響。⑤真實性:樣品中除HCPs以外的物質(zhì)在質(zhì)譜分析中同樣會產(chǎn)生質(zhì)譜信號,需要去除復雜的背景噪音避免假陽性和假陰性的出現(xiàn),建立合理標準的生信分析流程。分析流程建立過程中同樣需要建立嚴格的質(zhì)控QC標準,并通過后期不同方法進行驗證,確定其標準的真實性。
湖州申科HCP試劑盒開發(fā)經(jīng)抗原表征、抗體制備到體系驗證,全流程符合法規(guī)要求。浙江工藝特異型宿主細胞蛋白(HCP)殘留檢測試劑盒開發(fā)要求宿主檢測方法替換需橋接驗證,確保新舊方法結(jié)果一致性與可比性。廣東工藝特異型宿主細胞蛋白(HCP)殘留檢測抗體覆蓋率驗證
大腸桿菌具有遺傳性狀清晰,易于培養(yǎng)和控制,表達水平高,成本低,周期短等特點,是優(yōu)先的經(jīng)濟實惠的蛋白表達系統(tǒng),K-12系列和B系列菌株是工業(yè)規(guī)模上常用于生物工程的E.coli細菌株。K-12菌種、所衍生出的DH5α、Top10、JM109等菌株,可用于大量生產(chǎn)質(zhì)粒DNA并進一步制備細胞基因治療產(chǎn)品和病毒載體類疫苗。源于B系的菌株,如BL21,更適用于高效轉(zhuǎn)染表達載體和常規(guī)蛋白的表達,如:病毒蛋白、重組蛋白疫苗、細胞因子、酶類等產(chǎn)品。湖州申科生物針對這兩種菌株的特點,分別開發(fā)了E.coli表達菌HCP殘留檢測試劑盒和E.coli克隆菌堿裂HCP殘留檢測試劑盒。
廣東工藝特異型宿主細胞蛋白(HCP)殘留檢測抗體覆蓋率驗證
下一篇:
沒有了
相關(guān)新聞
- 廣東工藝特異型宿主細胞蛋白(HCP)殘留檢測抗體覆蓋率驗證 2025-08-25
- 重組蛋白用宿主細胞蛋白(HCP)殘留檢測 2025-08-25
- 廣東工藝特異型宿主細胞蛋白(HCP)殘留檢測 2025-08-25
- 廣東重組蛋白用宿主細胞蛋白(HCP)殘留檢測抗體制備 2025-08-25
- 廣東定制化宿主細胞蛋白(HCP)殘留檢測抗體制備 2025-08-25
- E.coli克隆菌宿主細胞蛋白(HCP)殘留檢測方法對比 2025-08-25
- 江蘇CHO宿主細胞蛋白(HCP)殘留檢測試劑盒 2025-08-25
- 北京單抗藥物用宿主細胞蛋白(HCP)殘留檢測抗體覆蓋率驗證 2025-08-25
- 北京生物制品宿主細胞蛋白(HCP)殘留檢測抗體覆蓋率驗證 2025-08-25
- ELISA法宿主細胞蛋白(HCP)殘留檢測常見問題分析 2025-08-25
推薦新聞
- 哪里有植物冠層光合氣體交換測量系統(tǒng) 2025-08-25
- 廣東工藝特異型宿主細胞蛋白(HCP)殘留檢測抗體覆蓋率驗證 2025-08-25
- 浙江智能中鹽核酸酶價格表 2025-08-25
- 浙江受體菌群移植廠商 2025-08-25
- 宿遷健康人工智能輔助診斷設(shè)備戰(zhàn)略 2025-08-25
- 吉林腦梗缺血預適應訓練儀功能 2025-08-25
- 蘇州一次性醫(yī)療監(jiān)測設(shè)備一站式制造服務(wù)大概多少錢 2025-08-25
- 阪美膠原蛋白肽口服液肽代工 2025-08-25
- 重組蛋白用宿主細胞蛋白(HCP)殘留檢測 2025-08-25
- 北京養(yǎng)心茶代理 2025-08-25