CHO-K1宿主細胞蛋白(HCP)殘留檢測供應廠家
來源:
發(fā)布時間:2025-08-23
宿主細胞蛋白來源中往往同時存在核酸,胞膜脂類,培養(yǎng)基中的氨基酸等非HCP成分會干擾總蛋白的檢測準確性,需要在檢測之前進行純化前處理,同時對總蛋白檢測方法進行方法學確認。HCP是一種多蛋白質(zhì)的混合物,總蛋白定量方法之間檢測結(jié)果會存在一定程度的差異,這也是導致HCP免疫檢測方法結(jié)果差異的原因之一。若HCP蛋白定量方法間檢測結(jié)果差異較大,一般同時采用2種以上經(jīng)過確認的方法檢測,再取均值??偟鞍讬z測方法的定量限一般只能達到μg/mL水平,但是HCP檢測試劑盒的產(chǎn)品校準品在ng/mL水平。從HCP高濃度原液稀釋到低濃度產(chǎn)品校準品中存在稀釋誤差,需要對產(chǎn)品校準品進行重新標定賦值。
湖州申科全自動 HCP ELISA 系統(tǒng)實現(xiàn)從加樣到檢測自動化,提升效率。CHO-K1宿主細胞蛋白(HCP)殘留檢測供應廠家
美國藥典<1132>章節(jié) 和歐洲藥典<2.6.34>章節(jié)建議對于即將進入商業(yè)化生產(chǎn)的(臨床III期及以后)或生產(chǎn)工藝穩(wěn)定的生物制品采用定制化ELISA試劑盒進行宿主細胞蛋白(HCP)殘留檢測,原因可能是:①確保檢測方法可以充分覆蓋實際工藝產(chǎn)生的HCPs,避免漏檢關鍵雜質(zhì);②支持更準確的免疫原性和安全性評估;③提供真實的工藝表征數(shù)據(jù),而非推測數(shù)據(jù);④滿足商業(yè)化生產(chǎn)質(zhì)量控制的方法一致性。此外,對目前市場上常見的HCP ELISA商業(yè)化試劑盒進行了測試,并與HCP ELISA定制化試劑盒進行對比,實驗結(jié)果發(fā)現(xiàn)不同商業(yè)化試劑盒檢測同一樣品的檢測值差異大,且準確性均低于定制化試劑盒,表明定制化試劑盒更能滿足產(chǎn)品質(zhì)量控制所需。
疫苗產(chǎn)品用宿主細胞蛋白(HCP)殘留檢測試劑盒開發(fā)要求湖州申科開發(fā)多種宿主 HCP 檢測試劑盒,提供抗體覆蓋率驗證服務。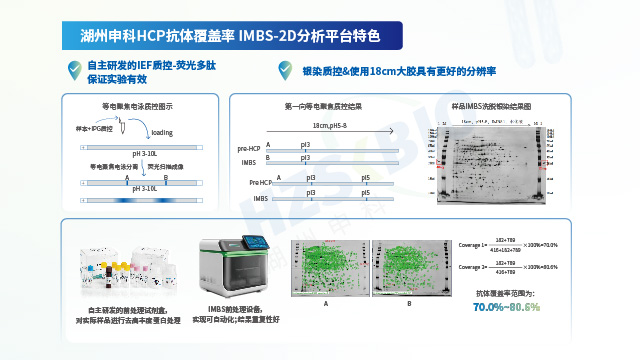
為了更好地控制工藝和保證產(chǎn)品質(zhì)量的穩(wěn)定,各國監(jiān)管機構(gòu)均要求提供使用的宿主細胞蛋白殘留檢測ELISA試劑盒的抗體覆蓋率數(shù)據(jù)。一般需進行覆蓋率分析的場景一般有以下幾種情況:①臨床II期后,若是繼續(xù)使用商品化試劑盒,則需要評估試劑盒抗體覆蓋率是否可以繼續(xù)用于質(zhì)量監(jiān)控;②臨床III期及以后階段,產(chǎn)品研究者開發(fā)了平臺化或工藝專屬型的HCP監(jiān)測方法,該類試劑盒在使用前要評估覆蓋率水平與商業(yè)化覆蓋水平的差異;③申報時沒有提交覆蓋率數(shù)據(jù),監(jiān)管機構(gòu)可能會對企業(yè)提出發(fā)補的要求;④產(chǎn)品上市后發(fā)生了包括生產(chǎn)場地變更,工藝變更,HCP分析方法變更等因素的變更,研究者則需要評估變更前后抗體覆蓋率水平的差異,以及該差異對藥品質(zhì)量與安全帶來的影響。
HCP是由宿主細胞(通常是哺乳動物細胞或微生物)產(chǎn)生的蛋白質(zhì)。這些蛋白質(zhì)具有潛在的風險,可能會影響藥物的安全性和有效性。因此,HCP殘留量是生物藥物中一個關鍵質(zhì)量屬性,要求在藥物的開發(fā)和生產(chǎn)階段對HCP的存在進行嚴格的監(jiān)控、管理和記錄。隨著生產(chǎn)流程,生物制品的純度在逐漸提高,HCPs總量和種類卻在持續(xù)降低,這使得對HCP的分析和監(jiān)測工作變得更加具有挑戰(zhàn)性。在這種情況下,開發(fā)高效的HCP富集材料和技術變得尤為關鍵。低豐度宿主殘留蛋白富集試劑盒,專為生物制品(如單抗、融合蛋白等)中HCP的富集和去除高豐度蛋白而設計,利用磁珠法構(gòu)建了一個多樣化且復雜的親和配體庫,旨在高效地識別并結(jié)合目標蛋白。其設計不僅針對傳統(tǒng)的單一蛋白,還能適用于融合蛋白、單克隆抗體等多種生物樣本類型,展現(xiàn)了較強的適用性和靈活性。
HCP 定制化開發(fā)需構(gòu)建成熟平臺、技術實力、合規(guī)體系、穩(wěn)定供應、專業(yè)團隊及成功案例的全維度支撐體系。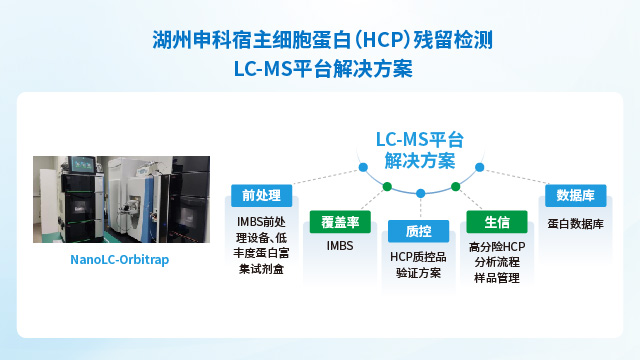
湖州申科生物致力于提供符合嚴格法規(guī)要求的宿主細胞蛋白(HCP)ELISA檢測試劑盒。為確保產(chǎn)品滿足生物制品(如抗體藥、疫苗)申報(如IND/BLA)的監(jiān)管標準,申科構(gòu)建了全流程依規(guī)開發(fā)的質(zhì)量體系:整個開發(fā)過程嚴格遵循ISO 13485質(zhì)量標準,并滿足用戶審計要求。其開發(fā)流程明確包含三個關鍵階段:①HCP殘留定量檢測參考品開發(fā):關鍵在于建立可靠的HCP抗原參考品,涵蓋抗原的表征、量值溯源與賦值、均一性和穩(wěn)定性考察等,確保檢測的準確性與代表性。②高質(zhì)量大批量抗體制備:通過優(yōu)化的HCP抗原動物免疫策略,結(jié)合嚴謹?shù)目贵w質(zhì)量標準(如建立標準、覆蓋率驗證)和穩(wěn)定的制備工藝,生產(chǎn)具有高特異性和廣覆蓋度的檢測抗體,保證檢測的特異性和靈敏度。③檢測體系開發(fā)及驗證:進行嚴謹?shù)臋z測體系開發(fā)與驗證工作,其驗證方案符合ICH指導原則及藥典關于分析方法驗證的標準要求。同時,嚴格執(zhí)行物料質(zhì)控,并在潔凈車間環(huán)境中進行生產(chǎn),確保試劑盒方法的穩(wěn)健性、重現(xiàn)性與法規(guī)符合性。這一從抗原源頭到成品體系的標準化、合規(guī)化開發(fā)流程,是湖州申科HCP檢測產(chǎn)品品質(zhì)與可靠性的根本保障。
湖州申科搭建高分辨蛋白質(zhì)譜技術平臺,結(jié)合IMBS技術,推出了IMBS-MS抗體覆蓋率評估方法。MRC-5宿主細胞蛋白(HCP)殘留檢測橋接驗證總蛋白檢測差異是 HCP 免疫檢測結(jié)果不同的原因之一。CHO-K1宿主細胞蛋白(HCP)殘留檢測供應廠家
LC-MS技術作為生物制品宿主細胞蛋白殘留檢測新趨勢,需考慮以下幾點:①穩(wěn)定性:需要HCPs LC-MS檢測流程進行驗證,全流程都需要有嚴格的QC控制,確保檢測結(jié)果的一致性和穩(wěn)定性。②可重復性:不同類型生物制品中HCPs提取效率不同,不同人員操作存在差異,需要在上機前通過不同方法評估HCPs的提取效率,避免人為因素造成結(jié)果重復性差。③準確度:方法開發(fā)與驗證階段,通過設立內(nèi)標與定量算法,根據(jù)內(nèi)標響應回算得到HCPs的含量,確保定量結(jié)果的準確性。④抗干擾能力:高豐度蛋白和特殊基質(zhì)會對質(zhì)譜檢測產(chǎn)生影響,需要通過前處理手段對高豐度蛋白或特殊的基質(zhì)進行去除,以減少其對HCPs肽段在質(zhì)譜檢測時的影響。⑤真實性:樣品中除HCPs以外的物質(zhì)在質(zhì)譜分析中同樣會產(chǎn)生質(zhì)譜信號,需要去除復雜的背景噪音避免假陽性和假陰性的出現(xiàn),建立合理標準的生信分析流程。分析流程建立過程中同樣需要建立嚴格的質(zhì)控QC標準,并通過后期不同方法進行驗證,確定其標準的真實性。
CHO-K1宿主細胞蛋白(HCP)殘留檢測供應廠家
相關新聞
- 工藝特異型宿主細胞蛋白(HCP)殘留檢測免疫策略 2025-08-23
- 漢遜酵母宿主細胞蛋白(HCP)殘留檢測方法對比 2025-08-23
- 浙江BHK宿主細胞蛋白(HCP)殘留檢測 2025-08-23
- 浙江通用型宿主細胞蛋白(HCP)殘留檢測抗體制備 2025-08-23
- 北京CHO宿主細胞蛋白(HCP)殘留檢測常見問題分析 2025-08-23
- 江蘇通用型宿主細胞蛋白(HCP)殘留檢測橋接驗證 2025-08-23
- CHO-K1宿主細胞蛋白(HCP)殘留檢測供應廠家 2025-08-23
- HEK293宿主細胞蛋白(HCP)殘留檢測方法學驗證 2025-08-23
- HEK293宿主細胞蛋白(HCP)殘留檢測供應廠家 2025-08-23
- 浙江ELISA法宿主細胞蛋白(HCP)殘留檢測方法開發(fā) 2025-08-23
推薦新聞
- 江西葉綠素熒光成像系統(tǒng)產(chǎn)品 2025-08-23
- 上海胎牛血清 2025-08-23
- 徐州駝背矯正器支具常見問題 2025-08-23
- 去眼袋面部項目儀器代理價格 2025-08-23
- 青海耐用雅安藏茶價格優(yōu)惠 2025-08-23
- 福建靶向蛋白質(zhì)組學 2025-08-23
- 云南國內(nèi)中頻電刺激睡眠呼吸治療儀加盟 2025-08-23
- NA培養(yǎng)基的檢驗報告 2025-08-23
- 寶山區(qū)名優(yōu)加熱絲回路銷售電話 2025-08-23
- 黃石組織芯片免疫熒光特點 2025-08-23